🧫 실험실 기초 화학지식 (Basic Laboratory Chemistry Knowledge)
물질의 기본 개념 (Basic Concept of Matter)
물질의 상태
물질은 크게 고체(Solid), 액체(Liquid),기체(Gas)로 존재 함.
이들 상태는 온도와 압력에 따라 변화할 수 있으며, 각 상태에서 물질의 입자 배열과 에너지는 다름.
States of Matter
Matter exists primarily in three states: Solid, Liquid, and Gas.
These states can change depending on temperature and pressure. In each state, the arrangement and energy of the particles differ.
고체: 입자들이 고정된 위치에서 진동하며, 일정한 모양과 부피를 유지.
예: 얼음.
Solid: Particles vibrate in fixed positions, maintaining a definite shape and volume.
Example: Ice.
액체: 입자들이 서로 가깝지만 이동할 수 있어 일정한 부피는 있지만 모양은 일정하지 않음.
예: 물.
Liquid: Particles are close to each other but can move, so they have a definite volume but no definite shape.
Example: Water.
기체: 입자들이 멀리 떨어져 자유롭게 이동하며, 모양과 부피가 일정하지 않음.
예: 공기.
Gas: Particles are far apart and move freely, having neither a definite shape nor a definite volume.
Example: Air.
물질의 성질 (Properties of Substances)
물리적 성질: 물질이 화학적으로 변화하지 않으면서 나타나는 성질로, 색, 냄새, 밀도, 녹는점, 끓는점 등이 포함.
Physical Properties Physical properties are characteristics of a substance that can be observed or measured without changing its chemical identity.
These include color, odor, density, melting point, and boiling point.
화학적 성질: 물질이 다른 물질로 변하면서 나타나는 성질로, 연소성, 산화성, 부식성 등이 포함됨.
예를 들어, 철이 녹슬면 산화된 철(Fe₂O₃)로 변함.
Chemical Properties Chemical properties describe a substance's ability to undergo chemical changes and form new substances. Examples include flammability, oxidation, and corrosion.
For instance, when iron rusts, it transforms into oxidized iron (Fe₂O₃).
혼합물과 순물질 (Mixtures and Pure Substances)
순물질: 화학적으로 순수한 물질로, 일정한 조성과 성질을 가지고 있음.
원소(예: 산소, O₂)와 화합물(예: 물, H₂O)이 포함 됨.
Pure Substances A pure substance is chemically uniform and has a fixed composition and consistent properties.
It includes elements (e.g., oxygen, O₂) and compounds (e.g., water, H₂O).
혼합물: 두 가지 이상의 물질이 섞여 있는 상태로, 각 성분이 고유의 성질을 유지.
균일 혼합물(예: 설탕물)과 불균일 혼합물(예: 모래와 물)이 있음.
Mixtures A mixture consists of two or more substances combined, with each component retaining its individual properties.
Homogeneous Mixtures: Uniform in composition (e.g., sugar water). Heterogeneous Mixtures: Non-uniform composition (e.g., sand and water).
원자와 분자 (Atoms and Molecules)
원자의 구조
원자는 물질을 구성하는 가장 작은 단위로, 핵과 전자로 이루어져 있음. 핵에는 양성자(양전하)와 중성자(중성)가 있으며, 전자는 음전하를 가지고 원자핵 주위를 공전 .
Structure of an Atom
An atom is the smallest unit of matter, consisting of a nucleus and electrons. The nucleus contains protons (positive charge) and neutrons (neutral), while electrons (negative charge) orbit around the nucleus.
양성자(Proton): 양전하(+1)를 가지고 있으며, 원자의 종류를 결정.
원자 번호는 양성자의 수로 결정 됨.
Proton: Positively charged particle (+1) that determines the type of atom. The number of protons defines the atomic number.
중성자(Neutron): 중성으로 전하가 없으며, 원자의 질량을 결정하는데 기여 함.
Neutron: Neutral particle with no charge that contributes to the atom's mass.
전자(Electron): 음전하(-1)를 가진 입자로, 원자의 화학적 성질과 결합에 중요한 역할을 함.
Electron: Negatively charged particle (-1) that plays a critical role in chemical properties and bonding of the atom.
원자 번호와 질량수 (Atomic Number and Mass Number)
원자 번호(Atomic Number): 원자핵 속의 양성자 수를 나타 냄.
예를 들어, 수소의 원자 번호는 1, 산소의 원자 번호는 8.
Atomic Number: Represents the number of protons in the nucleus of an atom. For example: Hydrogen has an atomic number of 1. Oxygen has an atomic number of 8.
질량수(Mass Number): 원자핵 속의 양성자와 중성자의 합을 나타 냄.
예를 들어, 헬륨의 질량수는 4(2개의 양성자와 2개의 중성자)임.
Mass Number: The sum of protons and neutrons in the nucleus. For example: Helium has a mass number of 4 (2 protons + 2 neutrons).
동위원소(Isotopes)
동일한 원소지만 중성자 수가 다른 원자를 동위원소라고 함.
동위원소는 화학적 성질은 같지만, 물리적 성질(질량 등)은 다름.
예를 들어, 탄소-12(C-12)와 탄소-14(C-14)는 탄소의 동위원소 힘.
Isotopes are atoms of the same element with a different number of neutrons. They share the same chemical properties but have different physical properties, such as mass.
For example: Carbon-12 (C-12) and Carbon-14 (C-14) are isotopes of carbon.
분자(Molecule)
두 개 이상의 원자가 화학 결합에 의해 결합하여 형성된 입자를 분자라고 함.
분자는 원소의 고유 성질을 가지며, 그 특성은 결합된 원자의 수와 배열에 의해 결정 됨.
예를 들어, 물 분자(H₂O)는 두 개의 수소 원자와 한 개의 산소 원자로 이루어져 있음.
A molecule is a particle formed by the chemical bonding of two or more atoms.
Molecules retain the unique properties of the substance and are defined by the number and arrangement of their constituent atoms.
For example: A water molecule (H₂O) consists of two hydrogen atoms and one oxygen atom.
세로줄 = 족(Group): “가족이 같으면 성격도 비슷”
같은 족은 겉전자(가장 바깥 전자 수)가 같아요 → 반응 방식이 비슷해요.
예시
1족(알칼리금속): Li, Na, K… 물 만나면 잘 반응, 항상 +1이온 되려함.
17족(할로겐): F, Cl, Br, I… 독특한 냄새·살균성, 보통 −1이온 되려함.
18족(비활성기체): He, Ne, Ar… 이미 안정해서 거의 반응 안 함.
기억법: “족이 같으면 바깥전자가 같고, 그래서 성격이 닮았다.”
가로줄 = 주기(Period): “왼쪽→오른쪽으로 갈수록 성격이 조금씩 바뀜”
원자번호(=양성자 수)가 1씩 증가 → 전자를 한 자리씩 채워 넣음.
일반 경향(상온 기준, 예외는 있지만 흐름만 잡자)
원자 크기: 왼→오 작아짐 (핵이 전자를 더 세게 끌어당김)
금속성: 왼→오 약해짐 (오른쪽 끝은 비금속 많음)
전기음성도(전자 끌어당기는 힘): 왼→오 커짐
예시
같은 주기에서 Na → Mg → … → Cl → Ar로 갈수록
금속성 ↓, 비금속성 ↑, 반응 성향이 “금속 → 비금속”으로 부드럽게 변해요.
원자번호 = 양성자 수: “이 번호가 그 원소의 정체”
원자번호가 곧 주민등록번호 같은 것.
주기율표는 원자번호 순으로 배열돼요. (원자량이 아니라 원자번호!)
상자(원소 칸) 읽는 초간단 규칙
기호: H, C, O … (국제 약자)
원자번호(Z): 그 원소의 정체 (예: O는 8)
원자량: 무게 느낌(동위원소 평균) — 대략적인 질량 비교용
큰 구역만 기억해도 반은 먹고 들어간다
왼쪽·가운데: 대부분 금속(광택, 전기·열 잘 통함, +이온 되기 쉬움)
오른쪽 위: 비금속(전기 안 통함, −이온/공유결합 선호)
경계선 쪽: 준금속(반금속)(금속·비금속 중간 성질, 예: Si, Ge)
바깥전자(=가장 중요한 힌트)
겉전자 수 → 이온 전하/결합 방식을 예측하기 쉬워요.
1족: 겉전자 1개 → +1 잃기 쉬움
2족: 겉전자 2개 → +2 잃기 쉬움
17족: 겉전자 7개 → −1 얻기 쉬움
18족: 겉전자 8개(또는 2개, He) → 이미 안정
자주 묻는 것, 한 줄 요약
왜 모양이 계단처럼 생겼나?
s, p, d, f 오비탈 채우는 순서 때문에 블록으로 나뉘어요(왼쪽 s-블록, 가운데 d-블록, 오른쪽 p-블록, 맨 아래 f-블록).
가족(족) 성질이 왜 반복될까?
전자껍질 채우는 패턴이 반복되기 때문(=주기성).
바로 써먹는 미니 치트키
상온 기체: H₂, N₂, O₂, F₂, Cl₂, 그리고 He, Ne, Ar, Kr, Xe
물에 잘 녹는 이온(외우면 편함): 1족+, NH₄⁺, NO₃⁻, CH₃COO⁻(대부분 예외 적음)
금속 반응성: 같은 족에서 아래로 갈수록 대체로 ↑(예: Na < K < Rb)
할로겐 반응성: 같은 족에서 위로 갈수록 대체로 ↑(I < Br < Cl < F)
칸(원소 상자) 읽는 법
꼭 알아야 할 3가지만!
기호(Symbol): H, C, O 같은 약자 이름표.
원자번호(Z): 그 원소의 주민번호. = 양성자 수. (산소 O는 Z=8 → 양성자 8개)
원자량(상대원자질량): 평균 무게 감(질량). 자연에 있는 여러 동위원소 비율을 평균 낸 값.
단위는 “u(amu)”지만, 숫자 그대로 g/mol로도 씀(실험 계산에서 편함)
상자 하나를 읽는 순서(초간단)
기호 확인 → “어떤 원소인지”
원자번호 Z → 양성자 수 = (중성 원자라면) 전자 수
원자량 대략 반올림 → 중성자 수 ≈ (반올림한 원자량 − Z)
예) O(산소)
기호: O, Z=8, 원자량 15.999
(중성자 추정) 16 − 8 = 8개
(전자) 중성 원자면 8개, 이온 O²⁻이면 전자 10개
“원자량”을 더 쉽게
왜 소수점? → 동위원소 섞인 평균이라서!
예) 염소(Cl): 약 75%가 Cl-35, 25%가 Cl-37 → 평균 35.45
실험 계산(몰질량)에서는 보통 소수점 1~2자리로 사용: C: 12.01 g/mol, O: 16.00 g/mol 처럼.
상자에서 추가로 볼 수 있는 것들(표 종류에 따라 있음)
원소 이름: Hydrogen, Carbon …(한글판은 ‘수소, 탄소’)
상태 아이콘/색: 상온에 고체/액체/기체 표시
족/주기: 상단이나 테두리에 Group(족) / Period(주기)
전자배치: 1s² 2s² 2p⁶ …처럼 껍질에 전자 채운 순서
산화수(Valence): 흔히 만드는 이온/결합 전하 예시(+2, −1 등)
전기음성도, 융점/끓는점, 밀도 같은 물성(확장형 표)
이온/전하까지 10초 정리
중성 원자: 전자 수 = Z
양이온(+): 전자 잃음(Na → Na⁺ : 11→10전자)
음이온(−): 전자 얻음(Cl → Cl⁻ : 17→18전자)
예시 3종, 한 번에 감 잡기
Fe(철): Z=26, 원자량≈55.85 → 중성자 ≈ 56−26=30 전이금속, 산화수 다양(예: +2, +3), 자성·촉매 성질
Na(나트륨): Z=11, 원자량≈22.99 → 중성자 ≈ 23−11=12 1족 금속, 쉽게 Na⁺(물과 격반응)
Cl(염소): Z=17, 원자량≈35.45 → 중성자 ≈ 35−17=18 17족 할로겐, 쉽게 Cl⁻, 살균·산화력
요약 카드
Z(원자번호) = 양성자 수 = 원소 정체
전자 수(중성) = Z, 이온이면 전자 수 달라짐
원자량 ≈ 평균 무게 → 중성자 ≈ (반올림 원자량 − Z)
같은 세로줄(족)은 성질 비슷, 오른쪽 갈수록 비금속성↑
큰 구역
금속 (왼쪽·가운데 대부분)
겉모습: 반짝, 은색/회색 톤 많음.
성질 한 줄: 전기·열 잘 통함, 펴지고 늘어남(전성·연성), 전자를 잃어 양이온(+) 되기 쉬움.
일상 예: 구리선(전선), 알루미늄 호일, 철(건물·기계), 금·은(장식/전자재료).
화학적 습관: 산·물과 반응해 이온으로 나가기 쉬움(특히 1족·2족). 산화되기 쉬움.
주요 가족
1족(알칼리): Na, K… 물과 격하게 반응, +1 이온.
2족(알칼리토): Mg, Ca… +2 이온.
전이금속(가운데 넓은 구역): Fe, Cu, Ni… 여러 산화수 가짐, 촉매로도 활약.
자주 묻는 예외
수은(Hg): 액체 금속.
알루미늄: 산화막 때문에 겉은 잘 안 녹는 듯 보임(실제로는 반응성 꽤 있음).
수소(H): 1족 위에 있지만 비금속 (위치만 거기, 성질은 오른쪽 편에 가까움).
비금속 (오른쪽 위)
겉모습: 광택 없음(탁함), 여러 상태 존재(고체: C, I / 기체: O₂, N₂ / 액체는 브로민 Br).
성질 한 줄: 전기 잘 안 통함, 잘 부서짐, 전자를 얻어 음이온(−) 되거나 공유결합 선호.
일상 예: 산소(숨 쉬는 공기), 질소(질소충전·보호가스), 염소(소독), 탄소(연필심·그래파이트, 다이아몬드), 규소 산화물(유리 원료—단 규소 자체는 준금속).
화학적 습관: 금속과 만나면 이온결합, 비금속끼리는 공유결합(분자) 만드는 경향.
자주 묻는 예외
탄소(그래파이트): 비금속인데 전기 잘 통함(층 구조에서 전자가 움직임).
할로겐(17족): 반응성 강함(살균/산화제).
희가스(18족): 너무 안정 — 거의 반응 안 함(네온사인, 아르곤 용접가스).
준금속(반금속) (금속과 비금속 사이 경계—계단선 부근)
대표 멤버: B, Si, Ge, As, Sb, Te (상황에 따라 Po, At도 거론).
성질 한 줄: 반도체적 성질—금속처럼 전기가 통하기도, 비금속처럼 반응하기도.
일상 예: 규소(Si)는 반도체 칩·태양전지의 핵심, 게르마늄(Ge)도 전자재료. 붕소(B)는 내열유리/세라믹.
왜 중요?: 전도도 조절(도핑)이 가능해서 IT·에너지 산업의 핵심 재료.
초간단 “구역별 습관” 외우기
금속: “주고(+), 반짝, 잘 통함”
→ 전자를 주고(+), 광택 반짝, 전기·열 잘 통함
비금속: “받고(−), 탁함, 분자/공유”
→ 전자를 받아(−) 또는 공유, 겉은 탁함, 분자 만들기 쉬움
준금속: “사이·조절(반도체)”
→ 금속·비금속 사이 성질, 전기 조절 가능(반도체)
성질 변화의 큰 흐름(지형 읽기)
왼→오른쪽: 금속성 ↓, 전기음성도 ↑, 원자크기 ↓
위→아래: 원자크기 ↑, 금속성 ↑, 이온화에너지 ↓ → 그래서 왼쪽 아래는 “금속성 강·반응성 큰 금속”, 오른쪽 위는 “비금속성 강·반응성 큰 비금속(할로겐)”이 몰려 있어요. 맨 끝(18족)은 안정.
팁
이온 만들 경향
금속: Na → Na⁺, Ca → Ca²⁺
비금속: Cl → Cl⁻, O → O²⁻ (혹은 공유결합)
재료 선택
전선/열전도: 구리, 알루미늄(금속)
반도체/태양광: 규소, 게르마늄(준금속)
가스/산화제: 산소, 염소(비금속)
예외 경계는 외워두면 좋아요: H(비금속)·C(그래파이트 도전성)·Hg(액체 금속)
준금속(반금속) (금속과 비금속 사이 경계—계단선 부근)
대표 멤버: B, Si, Ge, As, Sb, Te (상황에 따라 Po, At도 거론).
성질 한 줄: 반도체적 성질—금속처럼 전기가 통하기도, 비금속처럼 반응하기도.
일상 예: 규소(Si)는 반도체 칩·태양전지의 핵심, 게르마늄(Ge)도 전자재료. 붕소(B)는 내열유리/세라믹.
왜 중요?: 전도도 조절(도핑)이 가능해서 IT·에너지 산업의 핵심 재료.
초간단 “구역별 습관” 외우기
금속: “주고(+), 반짝, 잘 통함”
→ 전자를 주고(+), 광택 반짝, 전기·열 잘 통함
비금속: “받고(−), 탁함, 분자/공유”
→ 전자를 받아(−) 또는 공유, 겉은 탁함, 분자 만들기 쉬움
준금속: “사이·조절(반도체)”
→ 금속·비금속 사이 성질, 전기 조절 가능(반도체)
유명한 “가족”(족)
1족 알칼리금속 (H 제외: Li, Na, K, Rb, Cs)
성격: 물 만나면 “펑!”—아주 활발(반응성 최상위)
이온: 항상 +1
일상/용도: Na → 소금(NaCl), Li → 2차전지(리튬이온)
모습: 은색·무른 금속, 공기·물과 금방 반응 → 기름 속 보관
TIP: “리나칼럽씨” (리튬–나트륨–칼륨–루비듐–세슘)
2족 알칼리토금속 (Mg, Ca, Sr, Ba…)
성격: 1족보단 얌전하지만 여전히 반응성 높음
이온: +2
일상/용도: Ca → 뼈/치아(탄산칼슘), Mg → 합금/소화제, BaSO₄ → X선 조영제
모습: 은백색 금속, 물과 반응(온수에서↑)
13족 붕소족 (B, Al, Ga, In, Tl)
성격: 금속·준금속 섞여 있음
이온: 주로 +3
일상/용도: Al(알루미늄) → 캔·창틀·가벼운 합금, B → 유리(붕규산유리), Ga → 반도체(LED)
특징: Al은 산화막 덕에 녹슬지 않는 느낌
14족 탄소족 (C, Si, Ge, Sn, Pb)
핵심: 탄소 C = 생명·유기화학의 중심
이온/결합: 산화수 다양(−4 ~ +4), 공유결합 왕성
일상/용도: C → 다이아·그래파이트·플라스틱, Si → 반도체/유리/실리콘, Sn → 주석도금, Pb → 납축전지(독성 주의)
포인트: Si는 지구 지각의 스타(규소, SiO₂)
15족 질소족(프닉토겐) (N, P, As, Sb, Bi)
성격: 비금속→금속성으로 변해감
이온/결합: 산화수 −3 ~ +5 다양(질소 화학 풍부)
일상/용도: N₂ → 공기 78%, P → 비료(NPK), As → 독성/반도체, Bi → 화장품·의약
포인트: N는 삼중결합(N≡N)으로 매우 안정—반응시키려면 에너지 필요
16족 산소족(칼코겐) (O, S, Se, Te…)
성격: 산화·환원 반응에 핵심
이온: 비금속일 때 주로 −2
일상/용도: O₂ → 호흡·연소, H₂O → 물, S → 고무가황·황산, Se → 광전소자
포인트: 산소는 산화의 주인공, 황은 냄새나는 화합물(황화물)과 친함
17족 할로겐 (F, Cl, Br, I, At)
성격: 독특한 냄새·강한 반응성, 살균 능력 Good
이온: −1(할라이드)
상태/색: F₂(옅은 노랑 기체, 매우 위험), Cl₂(녹황색 기체), Br₂(적갈색 액체), I₂(보라 고체·승화)
일상/용도: Cl → 소독, I → 갑상선 요오드, F → 불소코팅
주의: 독성·부식성 강함(취급 주의)
18족 비활성기체(희가스) (He, Ne, Ar, Kr, Xe, Rn)
성격: 거의 반응 안 함(전자껍질 꽉 참)
상태: 상온 기체
일상/용도: He → 풍선·초전도 냉각, Ne → 네온사인, Ar → 용접·보호가스
포인트: 실험에서 불활성 분위기 만들 때 최애
전이금속(3~12족: Fe, Cu, Ni, Zn, Ag, Au, Pt…)
성격: 여러 산화수, 착화합물, 촉매로 대활약
일상/용도: Fe(강철), Cu(전선), Ni(도금·배터리), Pt/Pd(촉매), Ag/Au(귀금속)
포인트: 자기·전기·촉매—공업의 중심
란탄족/악티늄족 (표 하단 두 줄)
란탄계(La~Lu): 희토류, 자석/레이저/LED/광자재
악티늄계(Ac~Lr): 대부분 방사성, 원자로·의료(동위원소)
요약
왼쪽 = 금속, 오른쪽 위 = 비금속, 가운데 = 전이금속
아래로 갈수록 원자 커지고 금속성↑,
오른쪽으로 갈수록 전자를 더 끌어당겨 비금속성↑
팁
금속(왼쪽): 아래로 갈수록 반응성 ↑ (K가 Na보다 더 세게 물 반응)
할로겐(오른쪽): 위로 갈수록 반응성 ↑ (F > Cl > Br > I)
안전
알칼리/알칼리토: 물 접촉 금지(수소+열, 폭발적)
할로겐: 흡입·접촉 주의(부식·독성)
전이금속 염: 일부 독성·환경영향(크롬(VI) 등)
같은 족(세로)에서 아래로 내려가면?
비유: 아파트 층이 늘어나는 것.
원자 크기↑ 층(전자껍질)이 늘어 → 전자가 핵에서 멀어짐.
금속성↑ 멀면 잡아당기는 힘이 느슨해져서 전자 내놓기 쉬움 → 금속성 커짐.
이온화에너지↓(전자 빼앗기 쉬움), 전기음성도↓(끌어당김 약함).
반응성
금속족(1·2족): 아래로 갈수록 반응성↑ (Li < Na < K …)
할로겐(17족): 아래로 갈수록 반응성↓ (F > Cl > Br > I)
이유: 전자 하나 더 받으려면 핵이 팍 끌어당겨야 하는데, 아래로 갈수록 멀고 가려져(차폐) 덜 세게 당김.
끓는점/녹는점
같은 족이라도 결합 종류에 따라 다양.
예) 17족(할로겐) 분자간 힘 ↑ → 아래로 갈수록 끓는점↑(F₂·Cl₂ 기체, Br₂ 액체, I₂ 고체).
👉 족 요약: “아래로 갈수록 멀고 둔감” (크기↑, 금속성↑, 금속 반응성↑ / 할로겐 반응성↓)
같은 주기(가로)에서 오른쪽으로 갈수록?
비유: 같은 층, 방만 바꾸는데 관리소장(핵)의 손아귀가 점점 세짐.
원자 크기↓
양성자 수(핵+)가 늘어 같은 층의 전자를 더 꽉 당김 → 작아짐.
금속성↓, 비금속성↑
전자를 내놓기보다 받거나 공유하려는 성질↑.
전기음성도↑, 이온화에너지↑
전자 잡고 놓지 않으려 함 → 빼앗기 어려움.
반응성
왼쪽 금속: 오른쪽 갈수록 반응성↓(내놓기 어려워지니까)
오른쪽 비금속: 오른쪽 갈수록 반응성↑(특히 17족)
단, 18족(희가스)는 이미 안정 → 거의 반응X.
👉 주기 요약: “오른쪽으로 갈수록 촘촘·깐깐” (크기↓, 금속성↓, 전기음성도↑)
왜 이런가?
껍질 수가 커지면: 전자가 멀어져 핵의 당김 약화(차폐↑)
같은 껍질에서 양성자 수가 늘면: 유효핵전하(끌어당김)↑ → 전자 꽉 잡음
대표 트렌드
원자반지름
↓ (같은 족) ---> ↑
→ (같은 주기) ---> ↓
이온화에너지(전자 뽑기 어려움)
↓ (같은 족) ---> ↓
→ (같은 주기) ---> ↑
전기음성도(전자 끌어당김)
↓ (같은 족) ---> ↓
→ (같은 주기) ---> ↑
금속성
↓ (같은 족) ---> ↑
→ (같은 주기) ---> ↓
반응성 금속: 아래로 갈수록↑, 왼→오른쪽으로 ↓
할로겐: 위로 갈수록↑ (F가 최강)
예시
Na vs K(둘 다 1족): K가 더 아래 → 크다, 전자 내놓기 쉬움 → 반응성 K > Na
Cl vs I(17족): 위로 갈수록 전자 잡는 힘↑ → 반응성 Cl > Br > I
C ~ F(같은 주기): 오른쪽 갈수록 작아짐, 전기음성도↑ → F가 전자를 가장 세게 당김.
예외/주의
전이금속(가운데 d블록)은 d전자 영향으로 트렌드가 부드럽지 않음(규칙 약함).
귀금속성/녹는점은 결합/격자 구조 영향이 커서 일반 트렌드와 다를 수 있음.
H(수소)는 1족 위에 있어도 금속 아님(특이 케이스).
희가스(18족): 전기음성도 표에서 보통 제외(이미 가득 참).
초간단
“아래로 갈수록 커지고, 느슨해지고, (금속은) 잘 튄다.”
“오른쪽으로 갈수록 작아지고, 깐깐해지고, 전자를 세게 끌어당긴다.”
K와 Na 중 누가 더 반응성 큰가? → K
Cl과 I 중 누가 더 반응성 큰가? → Cl
같은 주기에서 누가 더 작을까: Mg vs S → S(오른쪽이 더 작음)
껍질과 방: 전자가 들어가는 순서
껍질(shell) = 아파트 층 (1층, 2층, 3층… → 1, 2, 3, … 껍질)
오비탈(방) = 각 층의 방 종류
s방(최대 2명), p방(최대 6명), d방(최대 10명)…
입주(전자 채우기) 규칙
낮은 층부터 채운다 → 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p … (대략 이렇게 흐른다고만 이해하면 충분해요)
한 방엔 2명까지, p/d는 방이 여러 개라 합쳐 6/10명까지.
👉 그래서 초반 대략 2, 8, 8, 18…처럼 채워지는 느낌이 납니다(정확한 수학 공식이 아니라 “감”을 잡는 숫자예요).
‘겉전자(가장 바깥 전자)’가 성질을 좌우
화학 반응은 대부분 겉전자(Valence electron)로 일어납니다.
겉전자가 비슷하면 성질도 비슷해요.
예) 1족(가장 왼쪽)은 겉전자가 항상 1개 → 물과 격하게 반응, 금속성 강함(리튬·나트륨·칼륨 등).
예) 17족(할로겐)은 겉전자가 항상 7개 → 아주 반응성이 크고 -1 이온 되기 쉬움(염소·브롬 등).
예) 18족(비활성기체)는 겉껍질이 꽉 참 → 안정, 거의 반응 안 함(헬륨·네온·아르곤…).
왜 ‘주기’가 생길까?
전자를 낮은 에너지부터 차곡차곡 채우다 보면,
한 층(껍질)이 안정한 패턴으로 거의 꽉 차는 순간이 옵니다(= 비활성기체).
그 다음 원소는 바로 위층의 새 방을 다시 처음부터 채우기 시작해요.
→ 그러니 겉전자의 개수가 1부터 다시 늘어나며 반복되고, 성질도 줄마다 반복됩니다.
이게 바로 주기성(성질의 반복)이에요.
나트륨 Na(원자번호 11): [네온] 3s¹ → 겉전자가 1개(1족 성질)
마그네슘 Mg(12): [네온] 3s² → 겉전자 2개(2족 성질)
…
아르곤 Ar(18): [네온] 3s² 3p⁶ → 겉껍질 가득(18족, 안정)
다음 칼륨 K(19)은 새 층 4s¹로 시작 → 다시 1족 성질!
표 모양이 이렇게 생긴 이유
왼쪽~가운데(전이금속 포함): 금속이 많음(전자 내놓기 쉬움).
오른쪽 위: 비금속(전자 받거나 공유결합).
s-블록(왼쪽 2열), p-블록(오른쪽 6열), d-블록(가운데 넓은 구역)로 나뉘는 것도 전자가 s → p → d 순서로 채워지는 흐름과 딱 맞아떨어져서 그래요.
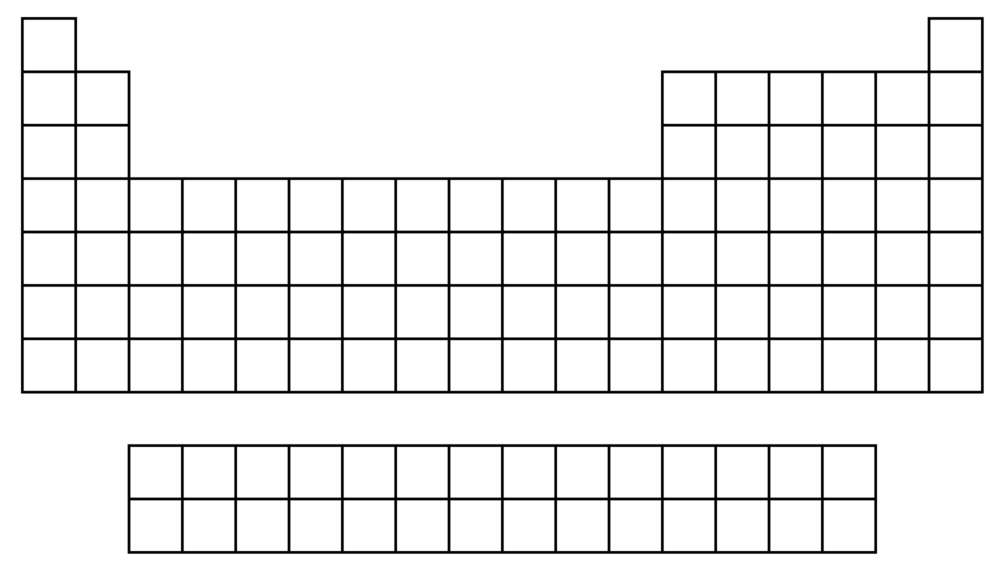
주기율표가 알려주는 쉬운 예측
이온 되기 쉬움?
1족(겉 1개) → +1 잘 됨. 2족 → +2 잘 됨.
17족(겉 7개) → 하나만 받으면 꽉 차니 −1 잘 됨.
크기 변화(원자 반지름)
아래로 갈수록 커짐(층이 늘어나니까).
오른쪽으로 갈수록 작아짐(핵이 전자를 더 세게 끌어당김).
반응성
금속(왼쪽): 아래로 갈수록 반응성↑(전자 내놓기 쉬워짐).
할로겐(17족): 위로 갈수록 반응성↑(전자 받기 더 쉬워짐, F가 최강).
초간단 팁
족 = 겉전자의 개수 패턴 → “성격 가족”.
주기 = 새 층 시작 → “층이 바뀌면 성격 리셋”.
끝 열(18족)은 꽉 찬 상태 → “너무 안정, 성격 무덤덤”.
왜 ‘주기’가 생길까?
전자를 낮은 에너지부터 차곡차곡 채우다 보면,
한 층(껍질)이 안정한 패턴으로 거의 꽉 차는 순간이 옵니다(= 비활성기체).
그 다음 원소는 바로 위층의 새 방을 다시 처음부터 채우기 시작해요.
→ 그러니 겉전자의 개수가 1부터 다시 늘어나며 반복되고, 성질도 줄마다 반복됩니다.
이게 바로 주기성(성질의 반복)이에요.
나트륨 Na(원자번호 11): [네온] 3s¹ → 겉전자가 1개(1족 성질)
마그네슘 Mg(12): [네온] 3s² → 겉전자 2개(2족 성질)
…
아르곤 Ar(18): [네온] 3s² 3p⁶ → 겉껍질 가득(18족, 안정)
다음 칼륨 K(19)은 새 층 4s¹로 시작 → 다시 1족 성질!
예
Cl(염소)는 몇 족? 겉전자 몇 개?
→ 17족, 7개
K(칼륨)은 왜 1족 성질일까?
→ 새 층 4s¹ 시작이라 겉전자 1개
Ne(네온)이 반응성이 낮은 이유?
→ 겉껍질 가득(완전 안정)
3가지만 기억
족(세로) = 겉전자 수가 비슷 → 성질이 비슷
주기(가로) = 원자번호가 1씩 증가 → 오른쪽으로 갈수록 비금속성↑, 원자 크기↓
왼쪽은 금속, 오른쪽 위는 비금속, 가운데는 전이금속
“찾는 원소”를 파악하는 순서
족부터 본다
1족(알칼리): 물과 격하게 반응, +1
2족(알칼리토): +2
17족(할로겐): −1
18족(희가스): 거의 반응 X
주기 위치로 감 잡기
같은 주기에서 오른쪽 갈수록: 원자 작아짐, 전자 끌어당김↑, 금속성↓
세 가지 실무 태그 붙이기
산화수(가장 흔한 것): 1족 +1, 2족 +2, 13족 +3, 16족 −2, 17족 −1
전기음성도: 오른쪽·위로 갈수록 큼(F가 최강)
상태(상온): 대부분 고체, 액체=Hg(수은), Br(브롬), 기체=H, N, O, F, Cl, 귀족가스
외우기 한 줄: “1/2는 +1/+2, 17은 −1, 18은 조용(안정)”
치트키
상태(고체/액체/기체) – 상온(25°C) 기준
기체(11개): H₂, N₂, O₂, F₂, Cl₂, He, Ne, Ar, Kr, Xe, Rn
액체(2개): Br₂, Hg
나머지 대부분 고체
흔한 산화수(대표값)
1족: +1 (Na⁺, K⁺ …)
2족: +2 (Mg²⁺, Ca²⁺ …)
13족(Al, Ga…): +3 → Al³⁺ 기억!
16족(O, S…): 보통 −2(O²⁻), S는 다양(+6, −2 등)
17족(F, Cl…): −1(Cl⁻, Br⁻, I⁻)
전이금속(Fe, Cu, Ni…): 여러 산화수(Fe²⁺/Fe³⁺, Cu⁺/Cu²⁺)
결합 경향
금속 + 비금속 → 이온결합(NaCl)
비금속 + 비금속 → 공유결합(H₂O, CO₂)
금속 + 금속 → 금속결합(구리선)
반응성 방향
왼쪽 금속(1·2족): 아래로 갈수록 반응성↑ (Li < Na < K …)
17족 할로겐: 위로 갈수록 반응성↑ (I < Br < Cl < F)
예시로 바로 익히기
Na(나트륨) 찾기
1족, 3주기 ⇒ +1 잘 내놓음, 금속성 강함
물과 반응해 NaOH + H₂↑ → 강염기성 생성
상태: 고체
Cl(염소)
17족, 3주기 ⇒ −1 받기 쉬움(Cl⁻)
강한 산화력(특히 기체 Cl₂), 소독제·PVC 원료
상태: 기체(분자 Cl₂)
Fe(철)
전이금속 구역 ⇒ 산화수 다양(Fe²⁺/Fe³⁺), 촉매·합금
산소·물과 반응해 녹 발생(Fe₂O₃·nH₂O)
상태: 고체
“족만 보고도” 성질 예측하기
1족(알칼리): 부드럽고 반응성↑, 물과 반응해 강염기 생성, 이온 반지름 큼
2족: 1족보다 반응성↓지만 역시 활발, +2
17족(할로겐): 독특한 냄새, 살균력, −1 음이온, 강산(HCl 등)과 연관
18족(희가스): 무색·무취·비활성(네온사인, 헬륨 풍선)
16족(산소족): O는 산소공급자, S는 냄새(황화물), −2 경향
전이금속: 색깔 있는 이온·복잡한 산화수·촉매(Fe, Cu, Ni, Pt…)
전기음성도/크기 감각, 한 장 요약
전기음성도: 오른쪽 위 클수록 큼(F > O > N ≈ Cl …)
원자 반지름: 왼쪽 아래 클수록 큼(Cs, Fr 근처가 큼)
이온 반지름: 전자를 잃으면 작아지고(양이온), 얻으면 커짐(음이온)
공식: “F는 전자욕심 1등, Cs는 몸집 1등”
실무에서 바로 쓰는 질문
이 원소는 금속/비금속? → 결합·전도성 예측
가장 흔한 산화수는? → 화합물식·산염기 판단
상태(고/액/기)는? → 취급·보관·배관/용기 선택
전기음성도 차는? → 결합 성질(이온/극성 공유/비극성) 가늠
예외·함정
H(수소): 1족 자리에 있지만 금속이 아님, 비금속성 + 특수 케이스
He vs H: He는 18족(완전안정), H는 반응성 큼
B, Si, Ge: 준금속(반도체 재료)
Ag, Zn, Al: 산화수 패턴이 비교적 단순(Ag⁺, Zn²⁺, Al³⁺)
화학 결합 (Chemical Bonding)
화학 결합은 원자들이 안정한 전자 배열을 이루기 위해 전자를 주고받거나 공유하는 과정에서 형성 됨.
Chemical bonding occurs when atoms interact to achieve a stable electron configuration by transferring or sharing electrons.
이온 결합(Ionic Bond)
이온 결합은 금속 원자와 비금속 원자가 전자를 주고받음으로써 형성 됨.
전자를 잃은 금속 원자는 양이온(+), 전자를 얻은 비금속 원자는 음이온(-)이 되어 정전기적 인력으로 결합.
예: NaCl(염화나트륨).
Ionic Bond
An ionic bond is formed when a metal atom and a nonmetal atom transfer electrons.
The metal atom loses electrons to become a positively charged cation (+).
The nonmetal atom gains electrons to become a negatively charged anion (-).
These oppositely charged ions are held together by electrostatic forces.
Example: Sodium chloride (NaCl).
공유 결합(Covalent Bond)
비금속 원자들이 전자를 공유하여 결합하는 방식.
두 원자가 서로 전자를 공유하여 안정한 전자 배열을 이루며 결합이 형성 됨.
예: H₂, O₂, CO₂.
Covalent Bond
A covalent bond occurs when nonmetal atoms share electrons.
By sharing electrons, the atoms achieve a stable electron configuration.
This type of bonding creates molecules.
Examples: Hydrogen (H₂), Oxygen (O₂), Carbon dioxide (CO₂).
금속 결합(Metallic Bond)
금속 원자들이 자유 전자를 공유하는 결합으로, 전자가 금속 원자 사이를 자유롭게 이동 함.
이러한 결합은 금속의 전기 전도성과 연성을 설명.
Metallic Bond
A metallic bond involves the sharing of free electrons among metal atoms.
The electrons move freely between the metal atoms, creating a "sea of electrons."
This bonding explains the electrical conductivity and malleability of metals.

화학 반응과 방정식 (Chemical Reactions and Equations)
화학 반응은 물질이 화학적으로 변하여 새로운 물질을 생성하는 과정.
이때 원자는 재배열되지만, 원자의 종류와 수는 반응 전후에 변하지 않음.
이를 화학 방정식으로 나타.
Chemical Reactions
A chemical reaction is the process by which substances undergo chemical changes to form new substances. During this process, atoms are rearranged, but the type and number of atoms remain unchanged before and after the reaction. These transformations are represented using chemical equations.
화학 반응식
화학 반응을 간결하게 표현하기 위해 화학식으로 나타내는 식을 화학 반응식이라고 함.
반응물(Reactants)이 변하여 생성물(Products)을 형성하는 과정을 나타 냄.
Chemical Equations
A chemical equation is a concise way to represent a chemical reaction using chemical formulas. It shows how reactants transform into products.
예: 메탄의 연소 CH₄ + 2O₂ → CO₂ + 2H₂O
Example: Combustion of Methane
CH₄ + 2O₂ → CO₂ + 2H₂O
CH₄: 메탄 (반응물) / CH₄: Methane (Reactant)
O₂: 산소 (반응물) / O₂: Oxygen (Reactant)
CO₂: 이산화탄소 (생성물) / CO₂: Carbon dioxide (Product)
H₂O: 물 (생성물) / H₂O: Water (Product)
이 화학 반응식에서, 반응물과 생성물의 수가 균형을 이루도록 맞춰져 있으며, 이는 질량 보존의 법칙을 따름.
In this chemical equation, the quantities of reactants and products are balanced to follow the Law of Conservation of Mass, which states that matter cannot be created or destroyed in a chemical reaction.
몰 개념(Mole Concept)
몰은 화학에서 물질의 양을 측정하는 기본 단위.
1몰은 6.022 × 10²³개의 입자를 의미하며, 아보가드로 수라고도 함.
몰 개념을 사용하면 물질의 질량과 입자 수를 계산할 수 있음.
The Mole Concept
The mole is a fundamental unit in chemistry used to measure the amount of a substance.
1 mole = 6.022 × 10²³ particles, known as Avogadro's number. Using the mole concept, we can calculate the mass and number of particles in a substance.
농도와 용액 (Concentration and Solutions)
몰농도(Molarity, M): 용액 내의 용질의 농도를 나타내는 단위로, 용액 1리터(L)에 포함된 용질의 몰수로 정의 됨.
몰농도는 화학 실험에서 용액의 농도를 계산하고 용액을 제조할 때 자주 사용.
Molarity (M)
Molarity is a unit of concentration that expresses the number of moles of solute per liter (L) of solution. It is commonly used in chemical experiments to calculate and prepare solutions.
몰농도 공식: 몰농도(M) = 용질의 몰수(mol) / 용액의 부피(L)
Formula:Molarity (M) = Moles of solute (mol) / Volume of solution (L)
예시:
1몰의 NaCl(염화나트륨)을 1리터의 물에 녹였을 때 그 용액의 몰농도는 1M.
Example: If 1 mole of NaCl (sodium chloride) is dissolved in 1 liter of water, the molarity of the solution is 1 M 1M.
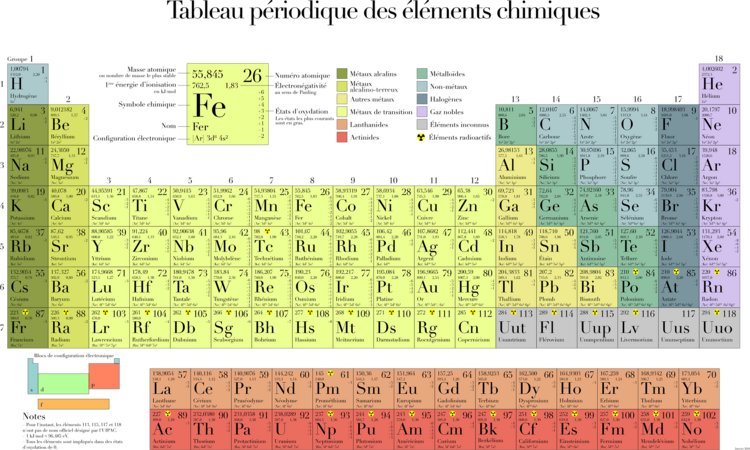
주기율표
주기율표는 원소들을 그들의 원자 번호(양성자의 수)에 따라 배열한 표로, 원소들의 성질을 예측하고 분류하는 데 중요한 도구.
주기율표는 원소들이 일정한 주기를 가지고 물리적·화학적 성질이 반복된다는 주기율에 기반을 두고 있음.
주기율표에서 원소들은 주기(Period)와 족(Group)으로 나뉨.
Periodic Table
The periodic table is a chart that organizes elements by their atomic number (number of protons), serving as an essential tool for predicting and classifying their properties.
It is based on the periodic law, which states that elements exhibit repeating patterns in their physical and chemical properties.
The elements in the periodic table are arranged in periods (horizontal rows) and groups (vertical columns).
주기율표의 기본 구조
Basic Structure of the Periodic Table
주기(Period)
주기율표의 가로줄.
총 7개의 주기가 있으며, 각 주기는 원자의 전자 껍질 수를 나타 냄.
예: 1주기에는 수소(H)와 헬륨(He)이 속하며, 이들은 모두 전자껍질이 하나 임.
Period
The horizontal rows in the periodic table. There are a total of 7 periods, and each period corresponds to the number of electron shells in an atom.
Example: Period 1 includes hydrogen (H) and helium (He), both of which have one electron shell.
족(Group)
주기율표의 세로줄.
같은 족에 속한 원소들은 비슷한 화학적 성질을 가짐.
1족(알칼리 금속): 리튬(Li), 나트륨(Na), 칼륨(K) 등.
17족(할로젠): 플루오린(F), 염소(Cl), 브로민(Br) 등.
18족(희귀 가스): 헬륨(He), 네온(Ne), 아르곤(Ar) 등.
The vertical columns in the periodic table.
Elements in the same group share similar chemical properties.
Group 1 (Alkali Metals): Lithium (Li), Sodium (Na), Potassium (K), etc.
Group 17 (Halogens): Fluorine (F), Chlorine (Cl), Bromine (Br), etc.
Group 18 (Noble Gases): Helium (He), Neon (Ne), Argon (Ar), etc.
주기율표에서 원소의 구분
Classification of Elements in the Periodic Table
금속: 주기율표의 왼쪽에 주로 위치하며, 전기 전도성이 좋고, 고체 상태에서 연성과 전성이 큼.
예: 철(Fe), 구리(Cu), 알루미늄(Al).
Metals
Located mostly on the left side of the periodic table. Known for high electrical conductivity, malleability, and ductility in the solid state. Example: Iron (Fe), Copper (Cu), Aluminum (Al).
비금속: 주로 오른쪽에 위치하며, 전도성이 낮고, 고체, 액체, 기체 상태로 존재할 수 있음.
예: 산소(O), 질소(N), 탄소(C).
Nonmetals
Found on the right side of the periodic table. Typically poor conductors and can exist in solid, liquid, or gas forms. Example: Oxygen (O), Nitrogen (N), Carbon (C).
준금속: 금속과 비금속의 중간 성질을 가진 원소들로, 주기율표의 금속과 비금속 경계에 위치함. 예: 규소(Si), 비소(As).
Metalloids
Possess properties of both metals and nonmetals. Found along the boundary between metals and nonmetals in the periodic table. Example: Silicon (Si), Arsenic (As).
주기율표에서 원소의 주요 성질
Key Properties of Elements in the Periodic Table
원자 번호(Atomic Number): 원자핵 속의 양성자의 수를 의미하며, 주기율표에서 원소는 원자 번호 순서대로 배열 됨.
Atomic Number: Indicates the number of protons in the nucleus of an atom. Elements are arranged in increasing atomic number.
원자 질량(Atomic Mass): 원자핵 속의 양성자와 중성자의 합.
주기율표에서는 각 원소의 평균 원자 질량을 나타 냄.
Atomic Mass: Represents the sum of protons and neutrons in an atom’s nucleus. The periodic table lists the average atomic mass of each element.
주기율표는 화학에서 중요한 역할을 하며, 원소의 성질과 반응성을 예측하는 데 유용한 도구.
온도와 압력의 영향
Effects of Temperature and Pressure
온도와 압력은 물질의 물리적 상태와 화학 반응에 큰 영향을 미치는 중요한 변수.
이 두 가지 요소는 화학 및 물리적 과정에서 물질의 상태, 반응 속도, 평형 상태 등 다양한 특성에 영향을 주며, 그 원리를 이해하는 것은 실험 및 공정에서 매우 중요.
Temperature and pressure are critical variables that significantly influence the physical state and chemical reactions of substances.
These factors affect various characteristics, such as the state of matter, reaction rates, and equilibrium conditions, making their understanding essential in experimental and industrial processes.
온도의 영향
온도는 물질의 분자 운동 에너지와 밀접하게 관련되어 있으며, 물질의 상태 변화와 화학 반응에 큰 영향을 줌.
온도가 물질의 상태에 미치는 영향
온도가 변하면 물질의 상태가 변화할 수 있음.
고체, 액체, 기체로 변하는 과정은 주로 온도에 의해 조절 됨.
Effects of Temperature
Temperature is closely related to the molecular kinetic energy of substances and plays a crucial role in both phase changes and chemical reactions.
Effect of Temperature on the State of Matter
Changes in temperature can lead to transformations between different states of matter.
The processes of solid, liquid, and gas transitions are primarily controlled by temperature.
융해(고체 → 액체): 고체는 열을 흡수하여 입자들이 더 빠르게 진동하고, 이로 인해 분자 간의 인력이 감소하면서 고체가 액체로 변함.
예: 얼음이 녹아서 물이 되는 과정.
Melting (Solid → Liquid): A solid absorbs heat, causing its particles to vibrate more vigorously. This reduces the intermolecular forces, leading to the transformation into a liquid.
Example: Ice melting into water.
기화(액체 → 기체): 액체가 기체로 변할 때는 더 많은 열을 흡수하여 분자들이 더 빠르게 움직이고, 이로 인해 액체가 증발하여 기체가 됨.
예: 물이 끓어서 수증기로 변하는 과정.
Vaporization (Liquid → Gas): When a liquid absorbs more heat, its molecules move faster, overcoming intermolecular forces and converting into a gas.
Example: Water boiling and turning into steam.
응고(액체 → 고체): 액체가 열을 잃고 분자 운동이 느려지면서 고체 상태로 변하는 과정입니다. 예: 물이 얼음으로 변하는 과정.
Freezing (Liquid → Solid): A liquid loses heat, reducing molecular motion and allowing the formation of a solid structure.
Example: Water freezing into ice.
응축(기체 → 액체): 기체가 열을 방출하고 분자 운동이 느려지면서 액체 상태로 변하는 과정입니다.
예: 공기 중의 수증기가 이슬로 응축되는 과정.
Condensation (Gas → Liquid): A gas releases heat, causing its molecular motion to slow down and transition into a liquid.
Example: Water vapor in the air condensing into dew.
온도가 화학 반응 속도에 미치는 영향
온도는 화학 반응 속도에 중요한 영향을 미침.
일반적으로, 온도가 증가하면 화학 반응 속도도 증가 함.
이는 충돌 이론과 관련이 있음.
Effect of Temperature on Reaction Rates
Temperature is a crucial factor in determining chemical reaction rates. Generally, an increase in temperature leads to an increase in the reaction rate.
This effect is explained by the collision theory.
충돌 이론
화학 반응은 반응물 입자들이 서로 충돌할 때 일어 남.
온도가 높아지면 분자들의 운동 에너지가 증가하고, 입자들이 더 빠르게 움직여 충돌 횟수가 많아지며, 더 많은 에너지를 가진 충돌이 일어나 반응이 더 쉽게 진행 됨.
Collision Theory: Chemical reactions occur when reactant particles collide with sufficient energy and proper orientation. At higher temperatures, molecules move faster due to increased kinetic energy, resulting in more frequent and energetic collisions.
반응 속도 증가: 온도 상승은 반응물 분자들의 운동 에너지를 증가시켜 충돌의 빈도와 강도를 높이므로 반응 속도를 증가시킴.
Increased Reaction Rate: A higher temperature raises the kinetic energy of molecules, increasing the frequency and intensity of collisions, which accelerates the reaction.
반응 속도 상수(k): 반응 속도는 속도 상수 k k로 표현되며, 이는 아레니우스 방정식으로 나타낼 수 있음.
Rate Constant (k): The reaction rate is represented by the rate constant k k, which is described by the Arrhenius equation.
k = A × e^(-Ea / RT)
k: 반응 속도 상수
A: 빈도 인자 (시도 횟수 상수 또는 충돌 빈도 상수)
e: 자연상수 (약 2.718)
Ea: 활성화 에너지 (반응이 일어나기 위해 필요한 최소 에너지)
R: 기체 상수 (8.314 J/mol·K)
T: 절대 온도 (켈빈, K)
온도가 증가하면 반응 속도 상수 k가 증가하여 반응이 빨라 짐.
방정식은 아레니우스 식으로, 반응 속도와 온도, 활성화 에너지 사이의 관계.
k는 온도가 높아질수록 증가하며, 활성화 에너지가 낮을수록 반응이 더 빨리 일어남.
e^(-Ea / RT)는 활성화 에너지를 초월하는 분자 비율을 나타냄.
온도가 화학 평형에 미치는 영향
온도는 르 샤틀리에의 원리(Le Chatelier's Principle)에 따라 화학 평형 상태에도 영향을 미침.
평형 상태에서는 반응물과 생성물이 일정한 비율로 존재하지만, 온도가 변화하면 평형이 이동하여 반응물이 더 많이 생성되거나 생성물이 더 많이 형성될 수 있음.
Effect of Temperature on Chemical Equilibrium
Temperature significantly impacts chemical equilibrium according to Le Chatelier's Principle. At equilibrium, reactants and products exist in a constant ratio, but a change in temperature can shift the equilibrium, resulting in either more reactants or more products.
흡열 반응(열을 흡수하는 반응): 온도가 증가하면 평형이 생성물 쪽으로 이동하여 반응이 더 많이 진행 됨.
즉, 흡열 반응에서는 온도를 높이면 더 많은 생성물이 생성 됨.
Endothermic Reactions (heat-absorbing reactions): When the temperature increases, the equilibrium shifts toward the products, driving the reaction forward.
Therefore, increasing the temperature in endothermic reactions leads to the formation of more products.
발열 반응(열을 방출하는 반응): 온도가 증가하면 평형이 반응물 쪽으로 이동하여 생성물의 양이 줄어 듬. 즉, 발열 반응에서는 온도를 낮추면 더 많은 생성물이 생성 됨.
Exothermic Reactions (heat-releasing reactions): When the temperature increases, the equilibrium shifts toward the reactants, reducing the amount of products. In exothermic reactions, lowering the temperature results in the formation of more products.
압력의 영향
압력은 주로 기체 상태의 물질에 큰 영향을 미침.
압력은 기체 분자들이 서로 충돌하는 빈도와 공간을 변화시켜 반응 속도와 평형에 영향을 미침.
압력이 기체의 상태에 미치는 영향 기체의 상태는 압력에 따라 크게 달라짐.
기체 상태에서 압력이 높아지면 기체 분자들이 더 좁은 공간에 몰려 밀도가 증가하고, 압력이 낮아지면 기체 분자들이 더 넓은 공간에 퍼지게 됨.
Effect of Pressure
Pressure mainly affects substances in the gaseous state and significantly influences reaction rates and equilibrium by altering the frequency of molecular collisions and available space.
Impact of Pressure on Gaseous States In gaseous systems, higher pressure forces gas molecules into a smaller volume, increasing density.
Conversely, lower pressure allows gas molecules to spread out into a larger volume.
보일의 법칙(Boyle's Law): 온도가 일정할 때, 기체의 부피는 압력에 반비례 함.
When temperature is constant, the volume of a gas is inversely proportional to its pressure.
P₁V₁ = P₂V₂
즉, 압력이 증가하면 부피는 감소하고, 압력이 감소하면 부피는 증가 함.
Implication: As pressure increases, volume decreases. As pressure decreases, volume increases.
압력이 화학 반응 속도에 미치는 영향
압력은 주로 기체 반응에서 반응 속도에 영향을 미침.
압력이 높아지면 기체 분자들의 농도가 증가하여 충돌 횟수가 많아지므로 반응 속도가 빨라 짐.
기체 반응에서는 반응물이 기체 상태일 때, 압력이 증가하면 반응 속도가 증가.
이는 반응물 분자들이 좁은 공간에 몰려 충돌이 더 빈번해지기 때문.
Effect of Pressure on the Rate of Chemical Reactions
Pressure primarily affects the reaction rate in gaseous reactions. When pressure increases, the concentration of gas molecules rises, resulting in more frequent collisions and, consequently, a faster reaction rate. For gaseous reactions where the reactants are in the gas phase, an increase in pressure leads to an increase in reaction rate. This is because gas molecules are compressed into a smaller volume, causing more frequent collisions.
압력이 화학 평형에 미치는 영향
압력은 르 샤틀리에의 원리에 따라 기체 반응의 화학 평형에 중요한 영향을 줌.
특히 반응물과 생성물이 모두 기체일 때, 압력의 변화는 평형 위치를 이동시킴.
Effect of Pressure on Chemical Equilibrium
Pressure has a significant impact on chemical equilibrium, particularly in gaseous reactions, as described by Le Chatelier's Principle. When both reactants and products are gases, changes in pressure can shift the equilibrium position.
기체의 부피가 감소하는 반응: 압력이 증가하면 평형은 부피가 더 작은 쪽으로 이동.
예를 들어, 반응에서 기체 분자의 수가 감소하는 쪽으로 평형이 이동.
Reactions where gas volume decreases: When pressure increases, the equilibrium shifts toward the side with fewer gas molecules.
예: N₂(g) + 3H₂(g) → 2NH₃(g)
이 반응에서 기체 분자의 수가 4개에서 2개로 줄어 듬.
따라서 압력을 증가시키면 암모니아(NH₃)의 생성이 증가 함.
In this reaction, the number of gas molecules decreases from 4 to 2. Therefore, increasing pressure favors the formation of ammonia (NH₃).
기체의 부피가 증가하는 반응: 압력이 감소하면 평형은 부피가 더 큰 쪽으로 이동.
즉, 기체 분자의 수가 증가하는 쪽으로 평형이 이동.
Reactions where gas volume increases: When pressure decreases, the equilibrium shifts toward the side with more gas molecules.
예:
2NO₂(g) → N₂O₄(g) 이 반응에서 기체 분자의 수가 2개에서 1개로 줄어듭니다. 따라서 압력을 증가시키면 N₂O₄의 생성이 증가하고, 압력을 감소시키면 NO₂의 생성이 증가 함.
In this reaction, the number of gas molecules decreases from 2 to 1. Hence, increasing pressure favors the formation of N₂O₄ , while decreasing pressure favors the formation of NO₂ .
열역학
열역학의 기본 개념
Thermodynamics: Basic Concepts
계(system)와 주변(environment)
계(system): 에너지를 주고받는 물리적, 화학적 실체를 말 함.
예를 들어, 실험할 때 사용하는 화학 반응 용기를 계라고 할 수 있음.
System: A physical or chemical entity that exchanges energy. Example: A chemical reaction vessel used in an experiment can be considered a system.
주변(environment): 계를 제외한 나머지 환경입니다. 계와 에너지를 주고받을 수 있는 부분.
Environment: Everything outside the system, which can exchange energy with the system.
계는 상호작용의 형태에 따라 나뉨
Types of Systems Based on Interaction
고립 계(Isolated System): 물질과 에너지가 계와 주변 사이에서 이동할 수 없는 계. 예: 열적으로 완전히 차단된 보온병.
Isolated System: Neither matter nor energy can be exchanged between the system and its surroundings. Example: A thermally insulated vacuum flask.
닫힌 계(Closed System): 에너지는 주고받을 수 있지만, 물질은 이동할 수 없는 계.
Closed System: Energy can be exchanged, but matter cannot move between the system and the surroundings.
열린 계(Open System): 물질과 에너지가 모두 계와 주변 사이에서 이동할 수 있는 계.
Open System: Both matter and energy can be exchanged between the system and the surroundings.
내부 에너지(U)
내부 에너지는 계 내에 저장된 총 에너지를 의미하며, 이에는 분자의 운동에너지와 위치에너지, 그리고 화학적 결합에 의한 에너지가 포함 됨.
Internal Energy (U) Internal energy refers to the total energy stored within a system. This includes the kinetic energy and potential energy of molecules, as well as the energy associated with chemical bonds.
내부 에너지(U)
내부 에너지는 계 내에 저장된 총 에너지를 의미하며, 이에는 분자의 운동에너지와 위치에너지, 그리고 화학적 결합에 의한 에너지가 포함 됨.
Internal Energy (U) Internal energy refers to the total energy stored within a system. It includes the kinetic energy and potential energy of molecules, as well as the energy associated with chemical bonds.
열역학 법칙
제1법칙
에너지 보존 법칙(First Law of Thermodynamics)
내용: 에너지는 생성되거나 소멸되지 않고, 단지 한 형태에서 다른 형태로 변환될 뿐 임.
즉, 에너지는 보존 됨.
Energy cannot be created or destroyed; it can only be transformed from one form to another. In other words, energy is conserved.
수식: ΔU = Q − W
ΔU 는 내부 에너지의 변화,
Q 는 계로 흡수된 열(양수) 또는 계로부터 방출된 열(음수),
W 는 계가 한 일(양수) 또는 계가 받은 일(음수)임.
예시: 화학 반응이 일어날 때, 반응이 흡열(열을 흡수) 또는 발열(열을 방출)하는 과정을 통해 내부 에너지 변화가 생김.
제2법칙
엔트로피 법칙(Second Law of Thermodynamics)
내용: 고립된 계에서 자연적으로 일어나는 모든 과정은 엔트로피(무질서도)가 증가하는 방향으로 진행 됨.
즉, 자발적인 과정에서는 계의 엔트로피가 감소할 수 없으며, 열은 차가운 곳에서 더운 곳으로 자발적으로 흐르지 않음.
Entropy and Natural Processes In an isolated system, all natural processes occur in a direction that increases entropy (degree of disorder). In other words, during spontaneous processes, the entropy of a system cannot decrease, and heat will not flow spontaneously from a colder region to a hotter region.
엔트로피(S): 엔트로피는 계의 무질서 정도를 나타내는 척도로, 엔트로피가 증가하면 무질서도가 커짐.
Entropy (S): Entropy is a measure of the degree of disorder in a system. When entropy increases, the level of disorder also increases.
예시: 얼음이 녹아서 물이 되는 과정에서, 물의 분자들이 더 자유롭게 움직이게 되어 엔트로피가 증가.
Example: When ice melts into water, the water molecules move more freely, resulting in an increase in entropy.
제3법칙
절대 영도 법칙(Third Law of Thermodynamics)
내용: 절대 영도(0K)에 도달하면, 완벽하게 결정된 순수 물질의 엔트로피는 0에 수렴.
즉, 절대 영도에서 물질의 분자 운동이 정지하게 되어 무질서도가 최소화 됨.
Third Law of Thermodynamics (Absolute Zero Law) Content: The Third Law of Thermodynamics states that as a system approaches absolute zero (0 K), the entropy of a perfectly ordered pure substance approaches zero. At absolute zero, molecular motion theoretically ceases, minimizing disorder to the greatest extent.
절대 영도(Absolute Zero): 0K(-273.15°C)는 이론적으로 분자의 운동이 완전히 정지하는 온도.
Absolute Zero (0 K): Absolute zero, equivalent to -273.15°C, is the theoretical temperature at which all molecular motion stops. This represents the lowest possible energy state of matter.
에너지 형태
열(Q)
열은 계와 주변 사이에서 이동하는 에너지의 한 형태로, 온도 차이에 의해 이동 함.
열은 단위 시간당 이동하는 에너지의 양을 말하며, 계가 열을 흡수하면 내부 에너지가 증가하고, 열을 방출하면 내부 에너지가 감소 함.
Forms of Energy
Heat (Q): Heat is a form of energy transferred between a system and its surroundings due to a temperature difference.
Heat transfer occurs as energy moves from a higher-temperature region to a lower-temperature region.
The amount of heat transferred per unit time determines the rate of energy flow.
When a system absorbs heat, its internal energy increases; when it releases heat, its internal energy decreases.
일(W)
일은 힘이 물체를 이동시키는 데 사용된 에너지를 말 함.
화학 반응에서도 일은 중요한 역할을 하며, 특히 계가 팽창하거나 압축될 때 일의 개념이 사용 됨.
팽창하는 계는 일을 함 (에너지를 잃음).
압축되는 계는 일을 받음 (에너지를 얻음).
Work (W): Work refers to the energy used to move an object by applying force.
In chemical reactions, work plays a vital role, particularly during the expansion or compression of a system.
Expanding System: Performs work (loses energy).
Compressing System: Receives work (gains energy).
열역학적 과정
등온 과정(Isothermal Process)
온도가 일정하게 유지되는 상태에서 일어나는 과정.
이 경우, 내부 에너지 변화가 없으며, Q = W 가 성립 함.
즉, 흡수된 열이 모두 일로 전환 됨.
Isothermal Process
An isothermal process occurs when the temperature remains constant throughout the process.
In this case, there is no change in internal energy, and the relationship Q=W holds. This means that all the heat absorbed is completely converted into work.
단열 과정(Adiabatic Process)
외부에서 열을 주고받지 않는 상태에서 일어나는 과정.
단열 과정에서는 내부 에너지 변화가 일로만 이루어 짐.
Adiabatic Process
An adiabatic process occurs when there is no heat exchange with the surroundings.
In an adiabatic process, changes in internal energy are solely due to work done.
ΔU = − W
ΔU: 내부 에너지의 변화 (Internal energy change)
− W: 일(work)에 의해 에너지가 빠져나감
내부 에너지의 변화(ΔU)는 시스템이 외부로 한 일(W)의 음수와 같음.
즉, 시스템이 외부로 일을 하면 내부 에너지가 감소한다는 의미
ΔU = − W
ΔU: Change in internal energy.
−W: Energy leaving the system as work. The change in internal energy (ΔU) is equal to the negative of the work (W) done by the system on its surroundings. In other words, when the system performs work on the surroundings, its internal energy decreases.
등압 과정(Isobaric Process)
압력이 일정하게 유지되는 상태에서 일어나는 과정.
이 과정에서는 흡수된 열이 온도 변화와 일로 나뉘어 나타 남.
Isobaric Process
An isobaric process is a thermodynamic process that occurs under constant pressure. In this process, the heat absorbed by the system is divided between causing a temperature change and doing work.
등적 과정(Isochoric Process)
부피가 일정하게 유지되는 상태에서 일어나는 과정.
이 경우, 계는 일을 하지 않으며, 흡수된 열은 모두 내부 에너지 변화에 사용 됨.
ΔU
=
Q
Isochoric Process
An isochoric process is a thermodynamic process in which the volume remains constant. In this case, the system does no work, and all the heat absorbed is used to change the internal energy.
ΔU = Q
깁스 자유 에너지(Gibbs Free Energy, G)
깁스 자유 에너지는 일정한 온도와 압력에서 화학 반응의 자발성을 예측하는 데 사용.
ΔG가 음수이면 반응이 자발적으로 일어날 수 있고, 양수이면 자발적으로 일어나지 않음.
Gibbs Free Energy (G)
Gibbs Free Energy is used to predict the spontaneity of a chemical reaction at constant temperature and pressure.
If ΔG is negative, the reaction can occur spontaneously.
If ΔG is positive, the reaction is non-spontaneous.
수식: ΔG=ΔH−TΔS
ΔG: 깁스 자유 에너지 변화,
ΔH: 엔탈피 변화,
T: 절대 온도(K),
ΔS: 엔트로피 변화.
예시: 발열 반응(열을 방출하는 반응)에서 엔트로피가 증가할 때, 깁스 자유 에너지는 음수가 되어 반응이 자발적으로 진행 됨.
Equation: ΔG = ΔH − TΔS
ΔG: Change in Gibbs free energy
ΔH: Change in enthalpy
T: Absolute temperature (in Kelvin)
ΔS: Change in entropy
Example: In an exothermic reaction (a reaction that releases heat), if the entropy increases, the Gibbs free energy becomes negative, indicating that the reaction proceeds spontaneously.
열역학적 평형
열역학적 평형은 계가 시간에 따라 더 이상 변하지 않는 상태입니다. 이 상태에서는 온도, 압력, 화학 성분 등이 일정하게 유지 됨.
열적 평형(Thermal Equilibrium): 계와 주변의 온도가 같아져 더 이상 열의 이동이 없는 상태.
역학적 평형(Mechanical Equilibrium): 계와 주변의 압력이 같아져 더 이상 부피 변화가 없는 상태.
화학적 평형(Chemical Equilibrium): 화학 반응이 두 방향으로 같은 속도로 일어나 생성물과 반응물의 농도가 일정하게 유지되는 상태.
Thermodynamic Equilibrium
Thermodynamic equilibrium refers to a state in which a system no longer changes over time. In this state, properties such as temperature, pressure, and chemical composition remain constant.
Thermal Equilibrium: The system and its surroundings reach the same temperature, resulting in no net heat transfer.
Mechanical Equilibrium: The pressure within the system and its surroundings are equal, preventing any change in volume.
Chemical Equilibrium: The chemical reactions occur at equal rates in both directions, maintaining constant concentrations of reactants and products.

상태 변화와 평형
화학에서 상태 변화와 평형은 중요한 개념으로, 물질의 상태 변화를 설명하고, 화학 반응에서 평형 상태를 분석하는 데 필수.
State Changes and Equilibrium
In chemistry, state changes and equilibrium are essential concepts that explain the transformation of matter and the analysis of equilibrium states in chemical reactions.
상태 변화
물질은 온도와 압력에 따라 상태가 변화할 수 있음.
State Changes Matter can undergo changes in state depending on temperature and pressure. State changes include:
상태 변화에는 융해(고체 → 액체), 응고(액체 → 고체), 기화(액체 → 기체), 응축(기체 → 액체) 등이 있음.
Melting (solid → liquid) Freezing (liquid → solid) Vaporization (liquid → gas) Condensation (gas → liquid)
화학 평형
가역 반응에서 반응이 정반대 방향으로 같은 속도로 진행될 때 화학 평형에 도달 함.
이때 반응물과 생성물의 농도가 일정하게 유지 됨.
평형 상수(K)는 특정 온도에서 반응물과 생성물의 농도 비율을 나타 냄.
Chemical Equilibrium In reversible reactions, chemical equilibrium is reached when the forward and reverse reactions occur at the same rate.
At this point, the concentrations of reactants and products remain constant.
The equilibrium constant (K) represents the ratio of the concentrations of products to reactants at a specific temperature.
실험 안전 지식
위험물 처리: 화학 물질은 독성, 인화성, 부식성 등의 위험을 가질 수 있으므로 적절한 보호 장비(장갑, 보안경, 실험복 등)를 착용해야 하며, 위험물 취급 시 주의가 필요.
Hazardous Material Handling: Chemical substances can possess risks such as toxicity, flammability, and corrosiveness. It is essential to wear appropriate protective equipment, including gloves, safety goggles, and lab coats, when handling hazardous materials. Proper caution must always be exercised.
화학 약품 보관: 산화제, 환원제, 산, 염기 등은 각각 적절한 조건에서 보관해야 하며, 서로 반응할 수 있는 물질은 구분하여 보관해야 함.
Chemical Storage: Oxidizers, reducers, acids, and bases must be stored under appropriate conditions. Substances that may react with each other should be separated to prevent unwanted reactions.
응급 처치: 화학 약품이 피부에 닿거나 눈에 들어간 경우 즉시 흐르는 물로 씻어내고, 필요한 경우 응급 처치를 받아야 함.
Emergency Procedures: In case of contact with hazardous chemicals on the skin or in the eyes, immediately rinse the affected area with running water. Seek medical attention if necessary.
화학 실험을 안전하고 정확하게 수행하기 위해서는 이러한 기본적인 화학 지식을 반드시 이해하고 있어야 함.
실험 전에 실험에 필요한 물질의 특성, 반응 메커니즘, 안전 절차 등을 이해하는 것이 중요하며, 실험 중 예상치 못한 사고를 예방할 수 있는 중요한 지침이 됨.
To conduct chemical experiments safely and accurately, it is essential to have a fundamental understanding of basic chemistry. Before performing any experiment, it is crucial to understand the properties of the substances involved, the reaction mechanisms, and the safety procedures. This knowledge serves as a critical guideline for preventing unexpected accidents during experiments.